Вещество в химии — физическая субстанция со специфическим химическим составом. В философском словаре Григория Теплова в 1751 году словом вещество переводился латинский термин Substantia.
Вещество в современной физике как правило понимается как вид материи, состоящий из фермионов или содержащий фермионы наряду с бозонами; обладает массой покоя, в отличие от некоторых типов полей, как например электромагнитное[1]. Обычно (при сравнительно низких температурах и плотностях) вещество состоит из частиц, среди которых чаще всего встречаются электроны, протоны и нейтроны. Последние два образуют атомные ядра, а все вместе — атомы (атомное вещество), из которых — молекулы, кристаллы и т. д. В некоторых условиях, как например в нейтронных звездах, могут существовать достаточно необычные виды вещества.
Вещество в биологии — материя, образующая ткани организмов, входящая в состав органелл клеток.
Агрегатные состояния вещества.
Вещество может существовать в трех агрегатных состояниях — твердом, жидком и газообразном.
При нагревании твердые вещества плавятся, а жидкости закипают, превращаясь в пар. Понижение температуры приводит к обратным превращениям. Некоторые газы при высоком давлении сжижаются. При всех этих явлениях мельчайшие частицы вещества не разрушаются. Таким образом, вещество, изменяя агрегатное состояние, не превращается в другое.
Каждый знает о трех агрегатных состояниях воды, в которых она существует в природе: лед, вода, водяной пар. Ho не всякое вещество может быть твердым, жидким и газообразным. Для сахара известны два агрегатных состояния: твердое и жидкое. При нагревании сахар плавится, затем его расплав темнеет, и появляется неприятный запах. Это свидетельствует о превращении сахара в другие вещества. Значит, газообразного состояния для сахара не существует. А такое вещество как графит нельзя расплавить: при температуре 3500 0C он сразу превращается в пар.
Кристаллические и аморфные вещества.
Если рассматривать соль и сахар через увеличительное стекло, то можно заметить, что крупинки соли имеют форму кубиков, а сахара — другую форму, но тоже правильную, симметричную. Каждая такая крупинка является кристаллом. Кристалл — это природное физическое тело, имеющее плоские грани (поверхности) и прямые ребра (стыки граней). Следовательно, соль и сахар — кристаллические вещества. К таким веществам относятся лимонная кислота, глюкоза, алмаз, графит, металлы и др. (рис. 23). Во многих случаях кристаллы веществ настолько мелкие, что их можно увидеть только под микроскопом.
Стекло — не кристаллическое, а аморфное1 вещество. Если его измельчить, то получим бесформенные кусочки, не похожие друг на друга. Аморфными веществами являются также крахмал, мука, полиэтилен и др. (рис. 24).
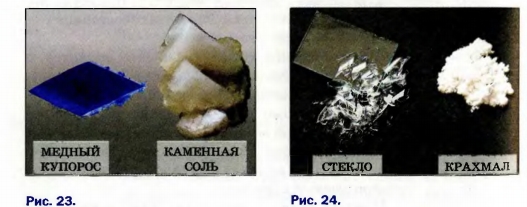
Рис. 23. Кристаллические вещества
Рис. 24. Аморфные вещества
Физические свойства веществ.
Все вещества чрезвычайно разнообразны; каждое обладает совокупностью определенных свойств.
Свойства вещества — это признаки, по которым вещество отличается от другого или подобно ему.
1 Термин происходит от греческих приставки а- и слова morphe — форма.
Железо легко отличить от древесины по цвету, особому блеску, а также на ощупь: металл всегда кажется более холодным, так как лучше проводит теплоту. Особенностью железа является то, что оно притягивается к магниту, а древесина — нет. В отличие от железа древесина в воде не тонет, поскольку ее плотность меньше плотности воды, а плотность железа — больше. Железо выдерживает высокую температуру, а древесина сначала темнеет, затем чернеет и загорается.
Свойства вещества, которые определяют наблюдением или измерением, без превращения его в другое вещество, называют физическими.
Важнейшие физические свойства вещества:
• агрегатное состояние при определенных температуре и давлении;
• цвет, блеск (или их отсутствие);
• запах (или его отсутствие);
• растворимость (или нерастворимость) в воде;
• температура плавления;
• температура кипения;
• плотность;
• теплопроводность;
• электропроводность (или неэлектропроводность).
Перечень физических свойств твердых веществ можно расширить, включив в него твердость, пластичность (или хрупкость), а для кристаллических — еще и форму кристаллов. Характеризуя жидкость, указывают, какая она — подвижная или маслянистая.
Такие физические свойства как цвет, запах, вкус, форма кристаллов можно определить визуально, с помощью органов чувств, а плотность, электропроводность, температуру плавления и кипения определяют измерением. Сведения о физических свойствах многих веществ собраны в специальной литературе, в частности — в справочниках.

Рис. 25. Нагревание иода
Физические свойства вещества зависят от его агрегатного состояния. Например, плотность льда, воды и водяного пара различна. Газообразный кислород бесцветный, а жидкий — голубой.
Знание физических свойств помогает «узнавать» немало веществ. Например, медь — единственный металл красного цвета. Соленый вкус имеет только поваренная соль. Иод — почти черное твердое вещество, которое при нагревании превращается в темно- фиолетовый пар (рис. 25). В большинстве случаев для определения вещества нужно при нимать во внимание несколько его свойств.
Лабораторный опыт№ 1
Ознакомление с физическими свойствами веществ
Вам выдано три пробирки, в которых содержатся селитра1, графит и полиэтилен2. В вашем распоряжении есть стакан с водой (или промывалка) и стеклянные палочки.
Опишите вещества. Каков характер частиц каждого вещества (кристаллики, порошок, мелкие кусочки произвольной формы)? Выясните, растворяются ли вещества в воде, легче они или тяжелее ее.
Какое свойство (свойства) позволяет отличить каждое вещество от двух других?
Назовите свойства, одинаковые для двух (трех) веществ.
Кроме физических свойств, каждое вещество имеет и химические свойства. О них пойдет речь позже.
1 Минеральное удобрение.
2 Учитель может заменить графит серой, медными или железными опилками, а полиэтилен — другим полимером.
Выводы
Вещество — то, из чего состоит физическое тело. Неотъемлемым признаком вещества является его масса.
Вещество может существовать в трех агрегатных состояниях: твердом, жидком и газообразном. Твердые вещества бывают кристаллическими и аморфными.
Свойства вещества — это признаки, по которым оно отличается от другого вещества или подобно ему.
Физические свойства вещества определяют наблюдением или измерением, без превращения его в другое вещество.

